Forschungs- und Innovationsprojekt
Ressourcenschonender Fruchtgemüseanbau im erdelosen Anbau im Gewächshaus mit größtmöglicher Rückstandsreduktion

Der Einsatz von chemischen Pflanzenschutzmitteln wird im gesellschaftlichen Diskurs kritisch gesehen. Die gärtnerische Praxis reagiert darauf zunehmend mit der Integration von biologischen und biotechnischen Maßnahmen gegen Krankheiten und Schädlinge. Die Impfung von Substraten mit mikrobiologischen Zusatzstoffen führt zu einer gesteuerten Wiederbelebung des Substrates. Mikroorganismen im Wurzelraum können dabei die Nährstoffumsetzung und den Transport positiv beeinflussen. Weiterhin spielen Mikroorganismen eine entscheidende Rolle im Bereich Gesundheit, Immunität und Resistenzen von Nutzpflanzen.
In der Praxis besteht zudem der Wunsch mineralische Substrate durch organische, nachwachsende Substrate, beispielsweise aus Kokos, Holzfaser oder Champost, zu ersetzen. Bislang fehlen jedoch eine objektive ökologische Bewertung und einheitliche Standards. Nachhaltigkeit und Umweltverträglichkeit lassen sich durch den CO2-Fußabdruck (Product Carbon Footprint) bewerten.
Ziel des Projektes
- Ökonomische und ökologische Bewertung der Varianten des Kulturverfahrens Fruchtgemüseanbau im erdelosen Anbauverfahren (Vergleiche von Steinwollverfahren, mehrjährig genutztes Perlit, einjährig und zweijährig verwendetes organisches Substrat).
- Recherchen zum tatsächlichen CO2-Fußabdruck. Bislang gibt es kein einheitliches objektives Verfahren zur Ermittlung eines CO2-Fußabdruckes.
- Weniger Pflanzenschutz und gesündere Pflanzen durch das Beleben des organischen Substrates (Antiphytopathogenes Potenzial).
- Bewertung nach phytopathologischen Kriterien. Das Projekt soll daher den Einfluss von Mikroorganismen sowohl auf die Pflanzengesundheit als auch auf die Ernährung der Pflanze transparenter machen.
- Erarbeitung einer Kulturanleitung für organische Substrate, mit dem Ziel einer rückstandsreduzierten und ressourcenschonenden Fruchtgemüseproduktion im Gewächshaus.
- Minimierung der Umwelteinträge aus dem erdelosen Kulturverfahren durch eine Anbauoptimierung.
Methode des Projektes
Die Projektziele sollen mit Hilfe von gartenbaulichen Versuchen erreicht werden.
Versuchsstandort Bamberg
Exaktversuche - Vergleich von mikrobiellen Bodenhilfsstoffen im erdelosen Anbau
Versuchsfrage 2016: Vergleich von mikrobiellen Bodenhilfsstoffen im erdelosen Tomatenanbau
| Bewässerungskreislauf 8.1. | Standard ohne mikrobiologische Zusatzstoffe |
| Bewässerungskreislauf 8.2. | NatuGro (Gesamtkonzept zur Förderung der biologischen Aktivität im Substrat) |
| Bewässerungskreislauf 7.1. | Bactiva & Endo Tray 10 x (Gesamtkonzept mikrobiologische Zusatzstoffe) |
| Bewässerungskreislauf 7.2. | Tmix (ein mikrobiologischer Zusatzstoff) |
Verfahren der Jungpflanzenanzucht
Es wurden im Versuch zwei Verfahren der Jungpflanzenanzucht, Kokospflanzwürfel der Firma Jiffy Products GmbH mit Steinwollwürfel der Firma Grodan, verglichen.
Als Substrat wurde Kokos (Forteco, Van der Knaap Gruppe) und als Kultur Tomate (Sorte 'Mecano' veredelt auf Unterlage 'Maxifort') gewählt.
Ergebnisse
In der unbehandelten Kontrollvariante wurde auf dem Steinwollwürfel mit 32 kg/m2 ein signifikant höherer Mengenertrag erzielt als auf dem Kokoswürfel mit 28,9 kg/m2 bei statistisch gleichem Stückertrag. Durch den Einsatz der mikrobiologischen Bodenzusatzstoffe gleichen sich die Erträge zwischen den beiden Jungpflanzenanzuchtvarianten an.
Die statistische Verrechnung ergab in der Varianten Bactiva (Kokospflanzwürfel) einen signifikanten Ertragsvorteil gegenüber der unbehandelten Kontrollvariante (Kokospflanzwürfel). Dies legt die Vermutung nahe, dass es positive Wechselwirkungen zwischen Mikroorganismen und organischem Substrat gibt.
Der Einsatz von mikrobiologischen Bodenzusatzstoffen in den Varianten mit einem Steinwollpflanzwürfel führte zu keiner Ertragssteigerung. Tomatenpflanzen auf einen Kokospflanzwürfel wiesen zur Pflanzung eine geringere Wuchshöhe und einen geringfügig späteren Blühbeginn auf, als die auf einen Steinwollwürfel angezogenen Jungpflanzen.
| Ertrag kg/m2 | Ertrag Stück/m2 | Einzelfruchtgewicht Gramm | nichtmarktfähig Stück/m2 | |
| Bactiva (Kokospflanzwürfel) | 31,4 ab | 378 a | 81,9 a | 15,9 a |
| Bactiva (Steinwollpflanzwürfel) | 31,5 ab | 384 a | 81,1 abc | 17,7 a |
| Tmix (Kokospflanzwürfel) | 29,9 bc | 378 a | 78,3 bc | 17,7 a |
| Tmix (Steinwollpflanzwürfel) | 31,1 ab | 382 a | 81,1 abc | 16,7 a |
| NatuGro (Kokospflanzwürfel) | 31,2 ab | 380 a | 82,2 a | 11,1 ab |
| NatuGro (Steinwollpflanzwürfel) | 31,6 ab | 385 a | 82,0 a | 8,0 b |
| unbehandelt (Kokospflanzwürfel) | 28,9 c | 372 a | 78,0 bc | 11,3 ab |
| unbehandelt (Steinwollpflanzwürfel) | 32,0 a | 385 a | 81,7 ab | 8,2 b |
| Durchschnitt | 30,9 | 381 | 80,8 | 13,3 |
| Kleinste signifikante Differenz | 1,9 | 18 | 3,4 | 7,3 |
Unterschiedliche Ertragszahlen mit gleichen Buchstaben sind zufällig (stat. nicht abgesichert).
Versuchsfrage 2017: Vergleich von mikrobiellen Bodenhilfsstoffen im erdelosen Salatgurkenanbau
| Bewässerungskreislauf 8.1 | Standard ohne mikrobiologische Zusatzstoffe |
| Bewässerungskreislauf 8.2. | NatuGro (Gesamtkonzept zur Förderung der biologischen Aktivität im Substrat) |
| Bewässerungskreislauf 7.1. | Bactiva (ein mikrobiologischer Zusatzstoff) |
| Bewässerungskreislauf 7.2. | Tmix (ein mikrobiologischer Zusatzstoff) |
Substrate
- Organisches Kokossubstrat (Van der Knaap Gruppe/ Wateringen, Niederlande)
- Mineralisches Perlitsubstrat (Pull Rhenen B.V/ Rhenen, Niederlande)
Als Kultur wurden Schlangengurken (Sorte 'Proloog') im Zweisatzanbau gewählt. Auf den Einsatz von Fungiziden wurde komplett verzichtet. Mit Hilfe von kurzfristigen, etwa dreistündigen Bewässerungsausfällen und das Einstellen einer Lüftungstemperatur von mehr als 30 °C wurden abiotische Stresssituationen simuliert.
Biotischer Stress wurde mithilfe einer Inokulation mit Fusarium bzw. Pythium erzeugt, um Aussagen zum antiphytopathogenen Potenzial der geprüften Varianten zu erhalten.
Tastversuche
Tastversuche sind unwiederholt und sollen erste Anhaltspunkte für möglich Prüfvarianten für zukünftige aufwendigere Exaktversuche liefern.
Förderung des antiphytopathogenen Potenzials
Mithilfe eines Tastversuches wurde 2016 und 2017 die antagonistische Wirkung von mikrobiellen Bodenhilfsstoffen geprüft.
Methode
Jeweils acht Gurkenpflanzen wurden mit Pythium ultimum inokuliert. Als Substrat wurde Perlit gewählt. Die Impfung der Jungpflanzen erfolgt nach Anbieterabgaben.
2016 geprüfte mikrobielle Bodenhilfsstoffe
- Wilhelms Best (Wilhelms GmbH, Cloppenburg)
- Bactiva, Endo Tray 10x (Bactiva GmbH, Straelen)
- Tmix (Gerlach Natürliche Düngemittel GmbH & Co.KG).
2017 geprüfte mikrobielle Bodenhilfsstoffe
- Bactiva, Endo Tray 10 x (Bactiva GmbH, Straelen)
- Tmix (Gerlach Natürliche Düngemittel GmbH & Co.KG)
- NatuGro System (Koppert Deutschland GmbH, Straelen)
- Pro Grow 4250 (PROGRESS Agrar Handelsgesellschaft mbH, Tostedt)
- Pro Grow 3500 (PROGRESS Agrar Handelsgesellschaft mbH, Tostedt)
- Rhizo Vital (ABITEP GmbH, Berlin)
- Carbon Gold (Carbin Gold, Bristol Großbritanien)
Einfluss von mikrobiellen Bodenhilfsstoffen auf die Nährstoffverfügbarkeit für die Pflanze
2018 wird der Einfluss von mikrobiellen Bodenhilfsstoffen auf die Nährstoffverfügbarkeit für die Pflanze untersucht. Mithilfe einer EC-Wert Reduzierung wird ein Nährstoffmangel erzeugt.
Als Kultur wurde Salatgurke Sorte 'Proloog' gewählt. Die Mangelvariante wird mit einer Standardvariante verglichen.
| Variante A | Kontrolle |
| Variante B | Bactiva, Endo Tray 10 x (Bactiva GmbH/Straelen) |
| Variante C | Tmix (Intrachem Bio Deutschland/Bad Camberg) |
| Variante D | Pro Grow 3500 (Progress Agrar Handelsgesellschaft mbH/Tostedt) |
Substrat
- Kokos (Van der Knaap Gruppe/Wateringen, Niederlande)
- Kokos (Jiffy Products International BV/Moerdijk, Niederlande)
Düngung
Standard Düngerezept
- Haus 6.2.: Standard (EC 3,0)
- Haus 6.1.: Reduziert (EC 2,0)
Analytische Untersuchungen in Veitshöchheim

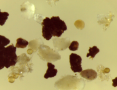
Pilzmycel von Fusarium sp. unter dem Mikroskop
Die Vielfalt der Mikroorganismen in Substraten und in der Rhizosphäre der Pflanzen ist für die Nährstofffreisetzung und die Nährstoffdynamik in den Substraten und damit auch für die Ernährung und Widerstandsfähigkeit der Pflanzen gegenüber abiotischem und biotischem Stress von grundlegender Bedeutung. Erdelose Substrate verfügen von Natur aus über eine vergleichsweise beschränkte Mikroorganismenflora. Es erscheint daher angeraten, die Belebung dieser Substrate mittels geeigneter Mikroorganismenpräparten zu initiieren und zu fördern. In diesem Forschungsvorhaben werden marktgängige Mikroorganismenpräparate eingesetzt und deren Verhalten vergleichend beobachtet und mikrobiologisch erfasst.
Ziele
- Charakterisierung der im Projekt eingesetzten Präparate zur biologischen Substrataktivierung
- Nachverfolgung der eingebrachten Mikroorganismen im Substrat, im Drainwasser und in den Wurzeln
- Prüfung der antiphytopathogenen Potenz der Präparate anhand von Modellversuchen
Methoden
 Zoombild vorhanden
Zoombild vorhanden
Probenahme an den Substratsäcken
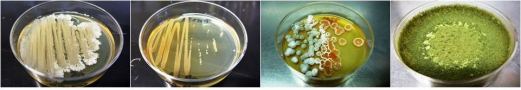
Für die Charakterisierung der Mikroorganismen, sowohl in den eingesetzten Präparaten als auch in den Substraten und im Drainwasser, werden Suspensionen in mehreren Verdünnungsstufen auf Nährmedien inkubiert. Die Substratproben müssen zuvor in einer Kugelmühle zerkleinert werden, damit eine homogene Suspension hergestellt werden kann. Durch Auszählen wird die Lebendkeimzahl bestimmt. Unterschiedliche Kolonien werden isoliert und weiter kultiviert. Anschließend werden sie morphologisch und mikroskopisch beurteilt und mit Hilfe von physiologischen Tests differenziert. Die daraus resultierenden Bestimmungen der Mikroorganismen werden durch molekularbiologische Sequenzierung abgesichert.
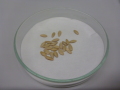
Von den Präparaten, die Endomykorrhizasporen enthalten, werden ebenfalls Suspensionen hergestellt. Diese werden über eine Siebkombination aufgetrennt. Nach der Auftrennung wird der Inhalt mikroskopisch auf das Vorhandensein von Sporen untersucht.
Erste Ergebnisse
| Präparat | Keimzahl- bestimmung Mittelwert (KBE/ml) | Keimzahlbestimmung Herstellerangabe (KBE/g) | qualitative Bestimmung nachgewiesener Mikroorganismen | qualitative Bestimmung Herstellerangaben |
|---|---|---|---|---|
| Tmix | 6,6x106 | keine Angaben | Trichoderma sp. Pseudomonas brassicacearum Bacillus amyloliquefaciens | Trichoderma Pseudomonas Streptomyceten Bacillus symbiontische Endomykorrhiza |
| Bactiva | 7,9 x 106 | 108 (Pilze) 108 (Bakterien) | Trichoderma sp. Bacillus amyloliquefaciens | Trichoderma harzianum T. reesei T. viride Gliocladium virens Rhizobakterien (PGPR) |
| Endodrip | 7,6 x 107 | 3x106 (Pilze) 2x109 (Bakterien) | Trichoderma sp Bacillus amyloliquefaciens Bacillus pumilus Bacillus licheniformis Endomykorrhizasporen | Trichoderma harzianum T. reesei T. viride Gliocladium virens Rhizobakterien (PGPR) |
| TH-Promotor | 5,2 x 106 | keine Angaben | Trichoderma sp. | Trichoderma spp. |
Substrate
Sämtliche Ergebnisse der Substratuntersuchungen basieren aktuell noch auf Einzelwerten und sind darum als vorläufig anzusehen.
Vegetationsperiode 2016
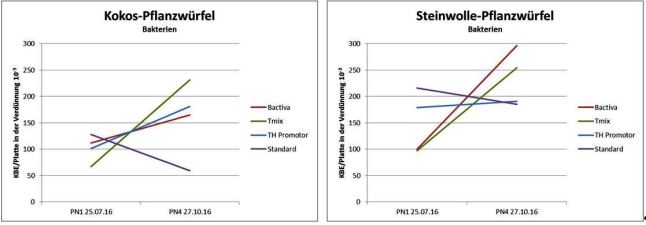
Die Bakterienkeimzahl steigt zwischen der ersten und der letzten Probenahme, sowohl in der Kokos- als auch in der Steinwollvariante an. Die Keimzahl fällt im Standard hingegen ab. Dies ist ein Hinweis darauf, dass sich Mikroorganismen im Vegetationszeitraum in den Kokossubstraten ansiedeln und vermehren können.
Neben anderen Gattungen werden überwiegend Bacillus sp. und Streptomyces sp. identifiziert.
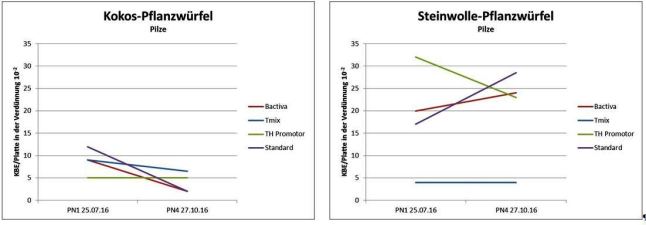
Die Gesamtkeimzahl der Pilze ist in den Steinwollvarianten meist leicht erhöht gegenüber den Kokosvarianten.
Allerdings wächst Trichoderma sp. in den Proben der Steinwollvarianten so gut wie gar nicht, wohingegen er in den Kokosvarianten durchaus isoliert werden kann.
Vegetationsperiode 2017
Im Kokossubstrat ist, im Gegensatz zum Perlit, bereits ohne Anwendung von mikrobiologischen Präparaten eine Mikroflora vorhanden, die überwiegend aus Bacillus sp. und Streptomyces sp. besteht.
Im Perlit konnten bislang nur sehr geringe Koloniezahlen isoliert werden. Weitere Untersuchungen müssen zeigen, ob Perlit überhaupt für die Ansiedelung von Mikroorganismen geeignet ist.
Modellversuche zur antiphytopathogenen Potenz der Präparate
 Zoombild vorhanden
Zoombild vorhanden
Inokulation der Gurkenpflanzen mit Pythium ultimum
Die Pathogenität des Inokulats wird an Gurkensamen in vitro überprüft. Hierfür wird ein Teil der Samen mit dem Überstand der Hirse-Wasser-Suspension mit Pythium ultimum , der andere Teil mit Leitungswasser, inkubiert.
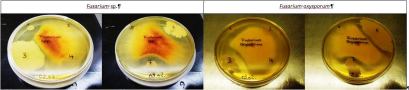
Um den Einfluss der isolierten Mikroorganismen aus den Präparaten gegenüber dem Phytopathogen Fusarium zu zeigen, werden sie zusammen auf einem festen Nährmedium inkubiert.
| 1 | Bacillus amyloliquefaciens | aus Tmix |
| 2 | Pseudomonas brassicacearum | aus Tmix |
| 3 | Bacillus amyloliquefaciens | aus Endodrip |
| 4 | Bacillus pumilus | aus Endodrip |
| 5 | Bacillus licheniformis | aus Endodrip |
| 6 | Bacillus amyloliquefaciens | aus Bactiva |
| 7 | Bacillus amyloliquefaciens | aus TH Promotor |
| Trichoderma atroviride | aus Tmix | |
| Trichoderma harzianum | aus TH Promotor |
Bei allen Bacillus amyloliquefaciens-Isolaten ist eine deutliche Hemmung gegenüber Fusarium sp. zu sehen, wohingegen Pseudomonas brassicacearum, Bacillus pumilus und Bacillus licheniformis das Phytopathogen nicht im Wachstum einschränken.
Trichoderma sp. breitet sich dominant über die Platten aus, bzw. überwächst sogar das Phytopathogen.
Eine abschliessende Bewertung zur antiphytopathogenen Potenz der eingesetzten Mikroorganismen kann zum jetzigen Zeitpunkt noch nicht abgegeben werden.
Ausblick
Die bisher erzielten Ergebnisse sind vielversprechend hinsichtlich einer umfangreichen Beschreibung der mikrobiologischen Vorgänge in den Substraten. Weitere Proben werden bearbeitet, um die getroffenen Aussagen abzusichern. Eine wesentliche Aufgabe dabei ist es, die Aktivität der Mikroorganismen zum Zeitpunkt der biotischen und abiotischen Stresssituationen zu erfassen, insbesondere, weil bei den mit Präparaten behandelten Varianten eine Ertragssteigerung im Falle des biotischen Stresses festgestellt werden konnte. Um die antiphythopathogene Potenz der eingesetzten Mikroorganismen zu beurteilen, ist ein Herausarbeiten des Auftretens und der Wirkung derselben notwendig. Durch die Untersuchung der gesammelten Drainwasserproben soll abgeschätzt werden, zu welchem Anteil die Mikroorganismen in den verschiedenen Substraten verbleiben, oder ob sie mit dem Drainwasser ausgespült werden.
Publikationen
Projektinformationen
Projektleitung: Gerd Sander (LWG-IEF), Oskar Kreß (LWG-IEF1), Josef Herrmann (LWG-A)
Projektbearbeiter: Martin Schulz (LWG-IEF 3), Bettina Barth (LWG-A3)
Laufzeit: 01.01.2016 bis 31.03.2019
Finanzierung: Bayerisches Staatsministerium für Ernährung, Landwirtschaft und Forsten (StMELF)
Projektpartner: Amt für Ernährung, Landwirtschaft und Forsten (AELF) Kitzingen-Gartenbauzentrum (GBZ) Bayern Nord, Hochschule Weihenstephan-Triesdorf (HWST), Erzeugerring für Gemüse Main-Dreieck e. V., Gemüseerzeugerring Knoblauchsland e. V.
Förderkennzeichen: A/16/01