Untypische Alterungsnote
Vermeidung der "Untypischen Alterungsnote" - Ascorbinsäure als wichtige Hilfe

Während der Reifung eines Weines kommt es üblicherweise zunächst zu einer positiven Entwicklung des Buketts, bis dieses mit zunehmendem Alter in Firne übergeht. Bei der „Untypischen Alterungsnote“ (UTA) im Wein handelt es sich dagegen um eine negative Veränderung des Aromas.
Diese, meist schon innerhalb eines Jahres nach der Gärung auftretende Fehlnote gab in Deutschland, wie in anderen weinbaubetreibenden Ländern, zunehmend Anlass zu Beanstandungen. Sensorisch wird die UTA mit unterschiedlichsten Begriffen, stets aber mit dem Fehlen des Sortenaromas beschrieben.
Die UTA tritt jahrgangsabhängig vor allem bei „kleinen“ Weinen früher Lesetermine, hoher Erträge und flachgründiger, trockengestresster Standorte auf. Der Weinausbau mit Ascorbinsäure ist keine Lösung für Probleme, die im weinbaulichen Bereich liegen. Er bietet aber die Möglichkeit, das frühzeitige Auftreten der untypischen Alterung der Weine zu verhindern. Nach positivem Vortest kann in jeder Ausbauphase des Weines Ascorbinsäure zur Qualitätserhaltung empfohlen werden.
Entstehung erst nach der Schwefelung
In einem Wein mit extremer UTA wurde mittels Gaschromatographie-Massenspektrometrie (GC-MS) 2-Aminoacetophenon (AAP) als eine verantwortliche Komponente für den Geruchseindruck UTA identifiziert (1). Mit verschiedenen analytischen und sensorischen Methoden konnte bestätigt werden, dass AAP die wesentliche verursachende Aromakomponente der UTA in Weißweinen ist, wobei hochsignifikante Korrelationen zwischen dem Gehalt an AAP und der UTA-Intensität festgestellt und durch Dotierungen mit der Reinsubstanz bestätigt wurden (2, 3). Die Schwellenkonzentrationen zur geruchlichen bzw. geschmacklichen Wahrnehmung liegt in wässriger Lösung bei 0,2 μg/l, in Weinen je nach Aromaprofil zwischen 0,5 bis 1,5 μg/l.
Aufgrund der chemischen Struktur von AAP wurde vermutet, dass diese Substanz aus der Aminosäure Tryptophan (TRP) bzw. aus Komponenten des Tryptophan-Stoffwechsels gebildet wird. Durch Versuche mit Modell-Lösungen, Traubenmosten und Weinen, die mit verschiedenen TRP-Stoffwechselprodukten dotiert wurden, konnte eine AAP-Bildung aus dem ubiquitär vorkommenden Wachstumshormon Indol-3-Essigsäure (IAA) bestätigt werden (4 ,5). Detaillierte Untersuchungen der Mechanismen dieser Umsetzung zeigten, dass AAP erst durch den Einfluss von schwefliger Säure auf IAA gebildet wird. Die Reaktion wird durch eine Kooxidation von schwefliger Säure und IAA gestartet, wobei Spuren von Sauerstoff in Superoxid- und/oder Hydroxylradikale umgewandelt werden, welche Sulfit zu Sulfat und IAA nach Ringspaltung über Formylaminoacetophenon zu AAP abbauen (6). Die Untersuchungsergebnisse entsprechen allen in der Praxis gemachten Erfahrungen zur Entstehung der UTA im Verlaufe des Weinausbaues, d.h. erst nach der Schwefelung.
HOENICKE (7) untersuchte Moste und daraus bereitete Weine dreier Jahrgänge (1996 bis 1998). Während IAA in den Mosten nur in gebundener Form in Konzentrationen zwischen < 20 und 130 μg/l nachweisbar war, wurden im Wein zwischen < 3 und 85 μg/l freie IAA analysiert. Der Anteil an gebundener IAA nahm dagegen während der Fermentation auf < 20 bis 35 μg/l ab. Die Mengen an freier IAA sind ausreichend, um auch bei niedrigen Umsetzungsraten zu sensorisch wahrnehmbaren Gehalten an AAP zu führen. Ziel aller Bemühungen in der UTA-Forschung war eine weinbauliche, zumindest aber kellerwirtschaftliche Lösung des UTA-Problems. Die Suche nach kellerwirtschaftlichen Möglichkeiten zur Vermeidung der UTA war zunächst wenig erfolgreich. Selbst durch die Verwendung von Trockenreinzuchthefen mit verstärkt fruchtigen Aromen oder durch niedrigere Gärtemperaturen konnte das Auftreten der UTA nur verzögert oder die Intensität vermindert werden (8).
Antiradikalisches Potenzial des Weines entscheidend
UTA ist bislang nie bei Rotweinen festgestellt worden; Vergleichbares trifft auf maischevergorene Weißweine und in vielen Fällen auf Weine aus der Pressfraktion (letzte 10 % der Mostmenge) zu. Aufgrund des zugrundeliegenden radikalischen Mechanismus der UTA-Bildung muss das antioxidative bzw. antiradikalische Potential des Weines eine entscheidende Rolle spielen. Dieses ist in Rotweinen, aber auch in Weißweinen mit hohem Polyphenolgehalt erhöht. Da eine direkte Bestimmung der antioxidativen Kapazität bei Mosten und Weinen in der Praxis sehr aufwendig ist, wurde als indirekte Methode der UTAFIX-Test zur Bestimmung des UTA-Potentiales entwickelt. Aufgrund aller Erkenntnisse unserer Untersuchungen zu den biochemischen Ursachen, den Mechanismen und den kellerwirtschaftlichen Einflüssen sowie der Tatsache, dass weinbauliche Lösungen nicht immer sicher greifen können, musste eine einfache kellerwirtschaftliche Methode gefunden werden, mit der die antioxidative Kapazität von Weißweinen verbessert wird. Insofern lag es nahe, Ascorbinsäure als einen, in der Lebensmittelindustrie in vielen Bereichen unverzichtbaren und auch in der Kellerwirtschaft zulässigen antioxidativen Zusatz als UTA-Inhibitor zu prüfen und einzusetzen.
Die Anwendung von Ascorbinsäure wurde 1965 mit der 9. Verordnung zur Ausführung des Weingesetzes in der BRD zugelassen. Der Zusatz bis zu einem Gehalt von 150 mg/l ist auf das Weinstadium begrenzt. Ascorbinsäure, auch Vitamin C genannt, zählt zu den am besten bekannten Verbindungen mit Schutzwirkung gegen Sauerstoff-Radikale. Unter Vitamin C werden Verbindungen eines mit dem Übergang von zwei Elektronen verbundenen Redoxsystems verstanden, das aus L-Ascorbinsäure, deren Monoanion Ascorbat, der in Form eines freien Radikals als Zwischenprodukt auftretenden Semidehydro-L-Ascorbinsäure und Dehydro-L-Ascorbinsäure besteht.
Ascorbinsäure ist aufs höchste sauerstoffempfindlich (9), die Oxidationsgeschwindigkeit ist vom pH-Wert abhängig. Wenn Metallionen wie Cu2+ oder Fe3+ die Reaktion katalysieren, liegen die Umsatzkonstanten um mehrere Größenordnungen höher als bei der nichtkatalysierten Oxidation, die Reaktionsgeschwindigkeit wird dabei vom Sauerstoffangebot vorgegeben. Die relativ gute Beständigkeit der Ascorbinsäure bei niedrigen pH-Werten ist für Lebensmittel und Speisen von entscheidender Bedeutung. Ähnlich wichtig sind für den Vitamin-C-Erhalt der Ausschluss von Schwermetallionen und die Hemmung der Diffusion bzw. die Entfernung von Sauerstoff (9, 10).
Die Hemmung des Ascorbinsäureabbaus in Fruchtsäften durch deren niedrigen pH-Wert sowie durch kupferkomplexierende Inhaltsstoffe ist seit den 50er Jahren bekannt (11). Ascorbinsäure gilt als wirkungsvolles Antioxidationsmittel im Lebensmittelbereich. Sie reagiert rasch mit dem Superoxidradikal (O2-), mit dem Perhydroxylradikal (HO2) und dem Hydroxylradikal (OH). Wasserstoffperoxid wird durch Ascorbinsäure reduziert und damit die Entstehung des reaktiven Hydroxylradikals verhindert (9, 12). Die Eigenschaften der Ascorbinsäure als Radikalfänger gelten heute als unbestritten und sind Gegenstand zahlreicher Untersuchungen und Publikationen. Beim Zusatz von Ascorbinsäure zu Getränken erhöht sich deren antioxidative Kapazität (13). In Wein kann Ascorbinsäure im Gegensatz zu Schwefeldioxid als Schutzfaktor gegen das Superoxidanion wirken (14). Das beim oxidativen Abbau der Ascorbinsäure auftretende Zwischenprodukt Diketogulonsäure stellt als Sauerstoff-Rezeptor ein noch besseres Reduktionsmittel für aggressive Sauerstoff-Spezies als die Ascorbinsäure dar.
Abbauweg der Ascorbinsäure von Rahmenbedingungen abhängig
So wird die Ascorbinsäure beispielsweise durch Wasserstoffperoxid über Dehydroascorbinsäure und Diketogulonsäure letztlich zu Tetrahydroxidiketohexansäure abgebaut (15). Andererseits kann in einer kupferinduzierten Ascorbinsäureoxidation Wasserstoffperoxid und das Hydroxylradikal entstehen. Diese, letztlich durch Kupfer-I-Ionen (Cu+) verursachte Reaktion findet in gleicher Weise statt, wenn andere Reduktionsmittel (z.B. Glutathion) zweiwertiges zum einwertigen Kupfer reduzieren (12). Peng et.al. (16) untersuchten die Bildung von Wasserstoffperoxid nach einem Zusatz von 200 mg/l Ascorbinsäure zu einem Wein der Rebsorte Colombard. Während im Ausgangswein keine Entstehung von Wasserstoffperoxid nachweisbar war, trat diese nach vollständiger Entfernung der Polyphenole und nach Zusatz von 5 mg/l Cu2+ (ca. 20 mg/l CuSO4) auf. In kupferhaltigen, unter Luftzutritt bei 45 °C gelagerten, polyphenolhaltigen Modellweinen wurde mit zunehmendem Ascorbinsäuregehalt eine Farbintensivierung und ein stärkerer SO2-Verlust festgestellt (16). Im Fruchtsaft- und Lebensmittelbereich kommt der kupferinduzierten Ascorbinsäureoxidation eine untergeordnete Bedeutung zu. Der Abbauweg der Ascorbinsäure wird wesentlich durch die Rahmenbedingungen bestimmt.
In wässriger, saurer Lösung entsteht ohne Luftzutritt vor allem Furfural und Kohlendioxid. Bei Luftkontakt läuft der Abbau unter Bildung von Wasser über Dehydroascorbinsäure, 2,3-Deketogulonsäure, L-Xyloson zu den Endprodukten 3-Hydroxy-2-pyron und 3-Furonsäure (17). Der einschlägigen Literatur ist eine Vielzahl weiterer Abbauprodukte zu entnehmen. Die Spaltprodukte der Ascorbinsäure und der Dehydroascorbinsäure sind entweder farblos oder braun gefärbt. Der unter aneroben Bedingungen auftretende wichtige, braungefärbte Metabolit Furfural gilt als Hauptursache für Farbveränderungen in Zitrussäften oder orangensafthaltigen Getränken während der Lagerung. Die Reaktionskinetik, der Ascorbinsäureverlust und die unterschiedlichen Zwischen- und Endprodukte der Umsetzung in sauren Getränken werden durch das Temperaturniveau und durch den verfügbaren Sauerstoffgehalt bestimmt (18 bis 23). Erhöhte Sauerstoffmengen und steigende Temperaturen beschleunigen den Ascorbinsäureabbau und beeinflussen die Bildung braungefärbter Metaboliten.
In Weinen kann ein Ascorbinsäurezusatz ebenfalls zur Farbintensivierung führen, wobei die Rebsorte von Bedeutung ist (24). Der Farbanstieg ist insbesondere dann ausgeprägt, wenn kein oder wenig Schwefeldioxid zugesetzt wurde. Aber selbst nach einer Gabe von 200 mg/l Schwefeldioxid zeichnen sich Unterschiede ab (16). Der Einfluss der Rebsorte auf das Bräunungsverhalten der Ascorbinsäure zeigt sich auch nach einem Zusatz zu Sekt nach dem Entfernen der Hefe: Nach einer Lagerdauer von elf Monaten bei 21°C war bei zwei von sechs Rebsortensekten eine verminderte, bei einem Sekt eine intensivere Braunfärbung erkennbar. Zu diesem Zeitpunkt waren noch 52 bis 70% des ursprünglichen Ascorbinsäuregehaltes vorhanden. In Verbindung mit einer schwachen Schwefelung (30 mg/l) trat bei keinem Sekt eine Braunfärbung auf. Nach einer zweitägigen Erwärmung auf 50°C unter Sauerstoffkontakt war in allen Ascorbinsäurevarianten eine stärkere Braunfärbung gegeben (25). In zwei Likörweinen mit hohem Restzuckergehalt reichten 50 mg/l Ascorbinsäure in einem Schnelltest (Zusatz von Wasserstoffperoxid, 40°C) unabhängig vom Gehalt an schwefliger Säure als Oxidationsschutz aus (26). Nachdem der Zusatz von Ascorbinsäure die Bildung von AAP verzögern oder verhindern kann, prüften wir während der letzten Jahre das Verhalten der Ascorbinsäure beim Ausbau gefährdeter Weine.
UTAFIX-Test
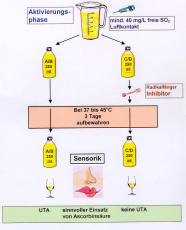 Zoombild vorhanden
Zoombild vorhanden
Würzburger UTAFIX-Test bei Verwendung von Ascorbinsäure
Ausbau von Weinen mit Ascorbinsäure
Ascorbinsäure bewirkt möglicherweise eine Verzögerung der Reifeentwicklung der Weine. Diese Wirkung könnte zu negativen Urteilen führen, wenn Weine ohne UTA-Potential erst verzögert ihre Trinkreife erreichen. Bei zwei von fünf Weinen wurde Ascorbinsäure kurz nach dem Zusatz im Dreieckstest erkannt und gesichert geringer bewertet. Der Einsatz von Ascorbinsäure sollte folglich immer nur dann erfolgen, wenn ein verstärktes UTA-Risiko vorliegt. Im Wein bereits vorhandenes AAP wird durch Ascorbinsäure nicht mehr entfernt oder maskiert. Daher ist ein erforderlicher Zusatz von Ascorbinsäure frühzeitig vorzunehmen. Die Anwesenheit von Kupferionen gilt als wichtigste Ursache für ein oxidatives Verhalten der Ascorbinsäure. In eigenen Versuchen mit Anbruchgebinden führte der Zusatz von Kupfersulfat (2 mg/l) zu keiner Beschleunigung des Ascorbinsäureabbaus. Ein Teil der schwefligen Säure wurde mit und ohne Kupfersulfat in Abhängigkeit vom Leerraum des Prüfgebindes oxidiert, die Ascorbinsäure übte dabei einen schwachen Schutz aus. Der Verlust an Ascorbinsäure variierte mit dem Leerraum, die Anwesenheit von Kupfer war von untergeordneter Bedeutung.
 Zoombild vorhanden
Zoombild vorhanden
Einfluß von Kupfersulfat auf das Oxidationsverhalten bei variierendem Leerraum
 Zoombild vorhanden
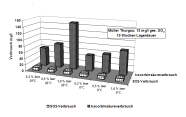
Zoombild vorhanden
Verbrauch an Ascorbinsäure und SO2 bei unterschiedlichen Temperaturen und variierendem Leerraum
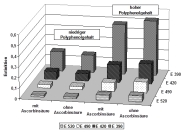 Zoombild vorhanden
Zoombild vorhanden
Farbintensität in Weinen mit und ohne Ascorbinsäurezusatz - 1997er Müller-Thurgau, 22 Monate bei 13 Grad Celsius
- ausreichender Gehalt an freier schwefliger Säure
- Ascorbinsäurezusatz unter Ausschöpfung des zulässigen Grenzwertes von 150 mg/l
- Vermeidung jeder unnötigen Luftaufnahme
Bei fünf verschiedenen Weinen prüften wir die Wirksamkeit einer Böckserbehandlung. Die Schönung mit Kupfersulfat erwies sich in Varianten mit und ohne Ascorbinsäure als effektiv. Die Neigung zu Kupfertrübungen ist in Weinen mit Ascorbinsäure größer als in herkömmlichen Weinen, die Gefahr wird jedoch häufig überschätzt. Vor allem muss die Trübungsneigung in Weinen mit einem Zusatz direkt vor der Abfüllung kritischer beurteilt werden, als wenn die Ascorbinsäuregabe in früheren Ausbaustadien stattfand. Ein zusätzlicher Eintrag von Kupferionen durch Süßreserve darf grundsätzlich nicht außer Acht gelassen werden.
Wichtig ist, dass Ascorbinsäure die Bestimmungen von freier schwefliger Säure stört. Es bedarf daher einer erweiterten Bestimmung, um die Konzentration an Ascorbinsäure und schwefliger Säure zu ermitteln. Für die in der Praxis gebräuchlichen Methoden läuft die Quantifizierung der schwefligen Säure und der Reduktone (weineigene Reduktone und Ascorbinsäure) in drei Schritten ab.
- Bestimmung der freien schwefligen Säure und Reduktone: Die Bestimmung wie üblich ohne besondere Zusätze durchführen.
- Bestimmung des Gehaltes an Reduktonen: Durch den Zusatz von 1 ml Glyoxal zu 25 ml Wein wird innerhalb von 5 Minuten die freie schweflige Säure gebunden. Bei der anschließenden, wie unter dem vorhergehenden Punkt angegebenen Bestimmung, erfasst man nur die Ascorbinsäure und sonstige Reduktone.
- Ermittlung des Gehaltes an „echter“ freier schwefliger Säure: Der Gehalt der ersten Bestimmung (der freien schwefligen Säure und Reduktone) abzüglich der zweiten Bestimmung (Reduktongehalt) ergibt den Gehalt an „echter“ freier schwefliger Säure.
Sensorische Beurteilung von Weinen mit und ohne Ascorbinsäurezusatz
 Zoombild vorhanden
Zoombild vorhanden
UTA-Bewertung bei 1989er Silvaner ohne und mit Ascorbinsäurezusatz im Jungweinstadium
Fazit
Der Weinausbau mit Ascorbinsäure ist keine Lösung für Probleme, die im weinbaulichen Bereich liegen. Er bietet aber die Möglichkeit, das frühzeitige Auftreten der untypischen Alterung der Weine zu verhindern. Nach positivem Vortest kann in jeder Ausbauphase des Weines Ascorbinsäure zur Qualitätserhaltung empfohlen werden.
Literatur
1. Rapp, G. Versini, H.A. Ullemeyer: 2-Aminoacetophenon: Verursachende Komponente der "Untypischen Alterungsnote" (Naphthalinton, Hybridton) bei Wein, Vitis 32, 61-62, 1993
2. N. Christoph, C. Christoph-Bauer, M. Geßner, H.J. Köhler: Die "Untypische Alterungsnote im Wein" Teil I: Untersuchungen zum Auftreten und zur sensorischen Charakterisierung
der "Untypischen Alterungsnote", Rebe & Wein 48, 350-356, 1995
3. M. Geßner, H.J. Köhler, N. Christoph, C. Christoph-Bauer, R. Miltenberger, A. Schmitt: Die "Untypische Alterungsnote" im Wein Teil II: Beschreibende Verkostung von UTA-Weinen: Beziehung zwischen Sensorik und chemisch-physikalischen Analysewerten, Rebe & Wein 48, 388-394, 1995
4. N. Christoph, C. Christoph-Bauer, M. Geßner, H.J. Köhler: Die "Untypische Alterungsnote im Wein" Teil VI: Untersuchungen zur Bildung von o-Aminoacetophenon aus Produkten des Trytophan-Stoffwechsels vor der alkoholischen Gärung. Rebe & Wein 49, 246-250, 1996
5. M. Geßner, H.J. Köhler, N. Christoph, C. Christoph-Bauer: Die "Untypische Alterungsnote im Wein" Teil VII: Untersuchungen zur Bildung von o-Aminoacetophenon aus Produkten des Trytophan-Stoffwechsels bei der alkoholischen Gärung. Rebe & Wein 49, 251-255, 1996
6. N. Christoph, C. Christoph-Bauer, M. Geßner, H.J. Köhler:, T.J. Simat, Hoenicke K.: Bildung von 2-Aminoacetophenon und Formylaminoacetophenon im Wein durch Einwirkung von schwefliger Säure auf Indol-3-essigsäure. Vitic. Enol. Sci. 53, 79-86, 1998
7. K. Hoenicke, A. Schwab, T.J. Simat, H. Steinhart: Bestimmung von freier und gebundener Indolessigsäure in Mosten und Weinen. Lebensmittelchemie, in Druck
8. H.J. Köhler, N. Christoph, C. Christoph-Bauer, M. Geßner, K.. Curschmann: Die "Untypische Alterungsnote" im Wein Teil V: Einfluß kellerwirtschaftlicher Maßnahmen auf die Ausprägung der UTA, Rebe & Wein 49, 213-218, 1996
9. Gassmann, B.: Vitamin C - Definition, Ernährungsphysiologie, Stoffwechsel, Versorgung und Versorgungszustand in der Bundesrepublik Deutschland. Ernährungsumschau 45, Nr. 8, 294 – 297, 1998
10. A. Agrawal, I. Rao, C. Gupta, S.K. Mishra, P.D. Sharma: ASCORBIC ACID – A POTENTIAL REDUCING AGENT IN AQUEOUS SOLUTION. Topics in chemistry series 1, 17, S 315-347, Jaipur 1992
11. J. Herrmann: Gibt es natürliche Hemmstoffe der Vitamin C-Zerstörung in den Fruchtsäften? Vortrag, Dresden, 1958
12. C.W. Bamforth, R.E. Muller, M.D. Walker: Oxygen and Oxygen Radicals in Malting and Brewing: A Review. ASBC Journal, 79 – 87, 1993
13. H. Dietrich: Bewertung der antioxidativen Kapazität von Fruchtsäften. GDCH-Seminar Fruchtsäfte und fruchtsafthaltige Getränke, Mainz 1998
14. N. Vivas, N. Saint-Cricq de Gaulejac, Y. Glories : Influence de SO2 et de l ´acide ascorbique sur l´activite antriradicalaire des tanins, mesuree sur l ´anion superoxyde. Application aux vins rouges. Vitis 36 (2), 91-96, 1997
15. J.C. Deutsch : Ascorbic Acid Oxidation by Hydrogen Peroxid. Analytical Biochemistry 255, 1-7, 1998
16. Z. Peng, B. Duncan, K.F. Pocock, M.A. Sefton: The effect of ascorbic acid on oxidative browning of white wines and model wines. Aust. Journal Grape Wine Res. 4, 127-135, 1998
17. J.-P. Yuan, F. Chen: Degradation of Ascorbic Acid in Aqueous Solution. J. Agric. Food Chem. 46, 5078-5082, 1998
18. M. Sawamura, K. Takemoto, Y. Matsuzaki, H. Ukeda, H. Kusunose: Identification of two Degradation Produkts from Aqueous Dehydroascorbic Acid. J. Agric. Food Chem. 42, 1200-1203, 1994
19. G.L. Robertson, C.M.L. Samaniego: Effect of Initial Dissolved Oxygen Levels on the Degradation of Ascorbic Acid and the Browning of Lemon Juice during Storage. J. Food Science 51, Nr. 1, 1986
20. M. Rodrique, G.D. Sadler, C.A. Sims, R.J. Braddock: Chemical Changes during Storage of an Alcoholic Orange Juice Beverage. Jour. Food Science 55, Nr. 2, 475-479, 1991
21. O. Solomon, U. Svanberg, A. Sahlström: Effekt of oxygen and fluorescent light on the quality of orange juice during storage at 8 °C. Food Chem. 53, 363-368, 1995
22. S.H. Lin, J. Agalloco: Degradation Kinetics of Ascorbic Acid. Process Biochemistry 9, 22-32, 1979
23. J.M. Smoot, St. Nagy: Effect of Storage Temperature and Duration of Total Vitamin C Content of Canned Single-Strength Grapefruit Juice. J. Agric. Food Chem. 28, 417-421, 1980
24. V. Panagiotakopoulou, J. R. Mowis : Chemical Additives to Reduce Browning in White Wines. Am. J. Enol. Vitic., Vol. 42, 3, 255-260, 1991
25. A. C. Marks, J.R. Morris: Ascorbic acid effects on the post-disgorgement oxidative stability of sparkling wine. Am. J. Enol. Vitic., Vol. 44, 2, 227-231, 1993
26. J. L. Favarel, E. Maffre, M. Jorieux, D. Bilières: Combinaison de l’anhydride sulfureux dans un vin de liqueur. Mise au point d’un test d’oxydation accé levée et application pour tester l’oxydabilité d’un vin de liqueur. Revue Francaise d’Oenologie, Paris (157), 39-45, 1996



